近日,武汉大学药学院闵昶课题组在国际化学期刊 JACS(Journal of the American Chemical Society)在线发表题为 “Scaffold Hopping of α,β-Unsaturated Ketones via Divergent Alkyl Amine Insertion” 的研究论文,通过氮插入策略实现α,β不饱和酮的多样性骨架编辑。
在药物化学领域,如何高效修饰分子骨架、快速得到结构类似物从而用于活性测试,始终是药物化学家们追求的核心目标之一。α,β-不饱和酮作为药物分子中的常见结构单元,其骨架的直接编辑一直是难点,传统反应多聚焦于外围基团修饰(如 1,2 - 或 1,4 - 加成),难以触及骨架核心结构的精准改造;传统的Schmidt反应实现的α,β-不饱和酮氮插入反应需使用剧毒的叠氮试剂,官能团耐受性差,更关键的是,其区域选择性严重依赖底物结构,无法满足药物研发中对分子骨架多样性的需求。针对上述痛点,研究团队开发了一种基于试剂控制的发散性骨架编辑策略,在温和的反应条件下实现了 α,β- 不饱和酮的 2,3 - 和 3,4 - 位区域选择性氮插入 —— 这一突破彻底摆脱了传统方法的局限。
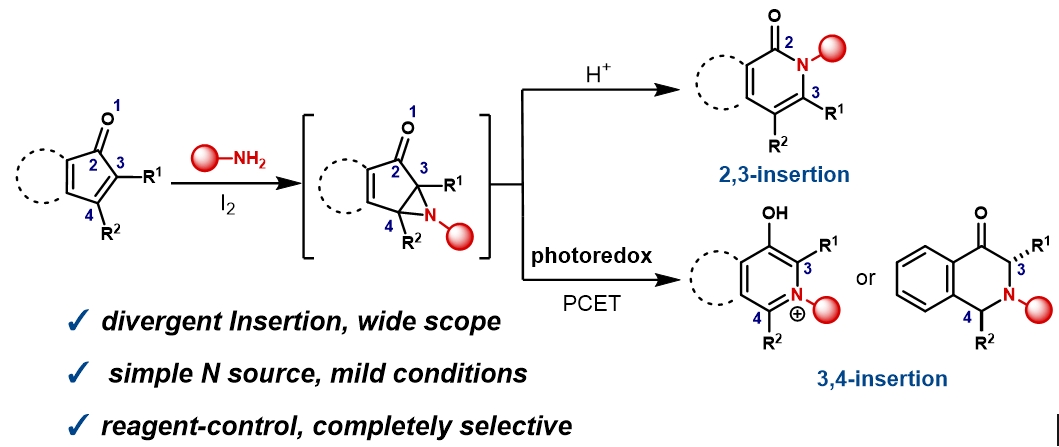
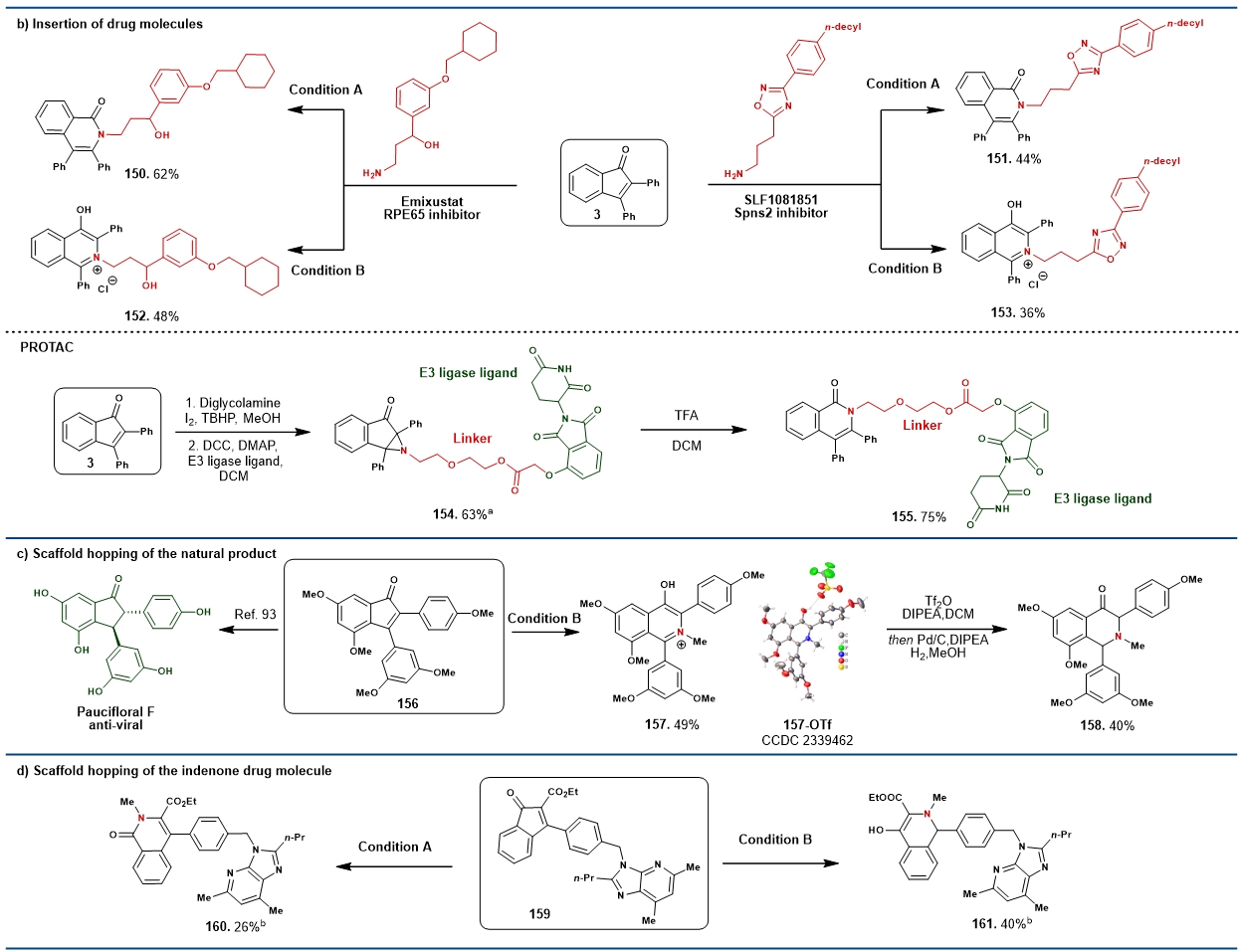
该策略展现了广泛的底物兼容性与实际应用价值,在药物研发场景,已经展现出应用潜力。例如对药物分子的直接插入:抗视网膜病变药物 Emixustat、Spns2 抑制剂 SLF1081851 的伯胺基团,可被区域选择性插入至目标位点,快速生成新的活性候选物,为药物分子设计提供了 "一键切换" 的高效工具;PROTAC 技术融合:传统PROTAC分子的设计中Linker多与小分子配体的外周官能团连接,该方法提供了将Linker嵌入目标底物分子骨架中的互补策略,丰富了PROTAC分子的多样性。天然产物修饰:抗病毒天然产物 Paucifloral F 的前体经 3,4 - 位插入反应后,可高效转化为含氮类似物,为天然产物的活性优化提供新思路;骨架跃迁突破:在 AT1 受体拮抗剂的合成中,传统方法需多步反应才能实现的异喹啉酮骨架,通过发散性氮插入骨架跃迁即可从茚酮完成转化得到目标活性化合物及结构类似物,显著提升合成效率。
该方法的开发,不仅解决了传统氮插入反应的安全性与效率问题,更重要的是为药物化学提供了一种 “精准调控” 的新策略 —— 通过可控的区域选择性插入,能从简单底物出发,快速构建结构多样的药物中间体库,大幅缩短从分子设计到活性筛选的周期,为高效发现候选药物奠定坚实基础。
武汉大学药学院博士生于慧光为论文第一作者,闵昶教授为论文唯一通讯作者,武汉大学为唯一通讯单位,以上研究工作得到武汉大学自主科研青年培育项目、武汉大学大型仪器设备开放补贴和武汉大学启动经费的支持。
文章链接:https://pubs.acs.org/doi/10.1021/jacs.5c06690